CAR-T新疗法使T细胞杀死癌细胞的能力提高了100 倍
CAR-T细胞疗法,也称为嵌合抗原受体T细胞免疫疗法,通过基因工程技术,改造患者自身的T淋巴细胞,使其能够更高效地识别和攻击肿瘤细胞。目前的CAR-T细胞疗法大多数只针对血液肿瘤和骨髓肿瘤,对于占据癌症总数90%的实体瘤,其治疗效果却不尽如人意。这一挑战使得如何提高CAR-T细胞疗法在实体瘤中的疗效成为了一个迫切需要解决的问题。
2024年2月7日,西北大学范伯格医学院皮肤病学和生物化学与分子遗传学副教授 Jaehyuk Choi 博士在Nature期刊发表了题为:Naturally occurring T cell mutations enhance engineered T cell therapies的研究论文。经过对导致淋巴瘤的恶性T细胞的突变进行深入研究,科学家们发现了一种名为CARD11-PIK3R3的特殊突变,该突变赋予了工程化T细胞卓越的效力。为了进一步增强正常人类T细胞的抗癌能力,研究者们将编码这一独特突变的基因植入这些细胞。令人惊喜的是,经过改造后的T细胞在消灭癌细胞方面的能力提升了超过100倍,且未显示出任何毒性反应。
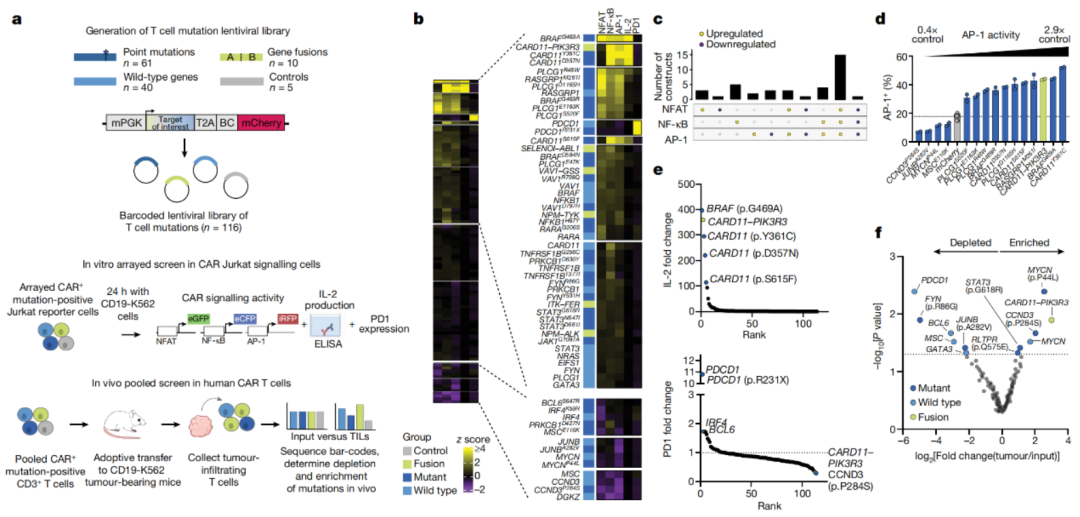
首先研究团队对T细胞肿瘤中发生的适应性突变进行筛选,生成了一个包含71个突变和45个野生型对照的基因文库。紧接着,他们将这些突变整合到人类和小鼠的T细胞中,进而筛选和评估它们对体外和体内T细胞表型的影响。
研究团队在CD4+皮肤T细胞淋巴瘤中发现了一种独特的基因融合——CARD11和PIK3R3的融合——称为CARD11-PIK3R3。携带这一基因突变的CAR-T细胞显著增加了AP-1和NF-κB信号转导、白介素-2(IL-2)的产生和体内外肿瘤杀伤作用。
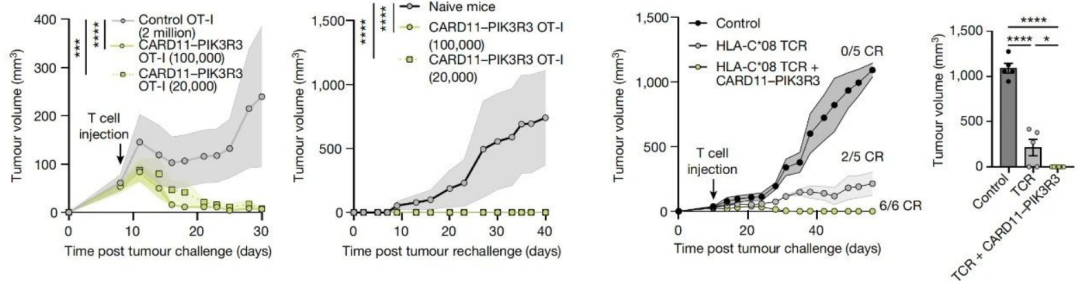
进一步研究表明,CARD11-PIK3R3以抗原依赖的方式增强了CARD11-BCL10-MALT1复合物信号通路,促进CAR-T细胞在几种对免疫疗法不敏感的肿瘤模型中的抗肿瘤疗效,并具有持久的肿瘤杀伤活性。
这项发表在《Nature》杂志上的研究揭示了淋巴瘤中天然存在的基因突变——CARD11-PIK3R3,能够显著提升CAR-T细胞对实体肿瘤的杀伤能力,增幅高达百倍。这一重要发现不仅为CAR-T细胞疗法在实体瘤治疗中的应用开辟了新的道路,同时也提示我们,探索和利用自然发生的基因突变可能为改进T细胞免疫疗法提供新的方向和思路。这一研究成果为未来的癌症免疫治疗领域带来了无限的可能性和希望。
原文链接:https://www.nature.com/articles/s41586-024-07018-7
推荐产品:人白介素2高表达NSG小鼠 CARD11抗体 PIK3R3抗体

